Oxygen (O₂) là một đơn chất khí trong nhóm phi kim thuộc chu kỳ 2 của bảng tuần hoàn. Đây là chất khí không màu, không mùi, không vị và đóng vai trò thiết yếu cho sự sống trên Trái Đất. O₂ chiếm khoảng 21% thể tích khí quyển và là tác nhân duy trì quá trình hô hấp, đốt cháy và nhiều phản ứng hóa học quan trọng.

Tính chất vật lý của Oxygen
|
Tính chất |
Mô tả |
|
Trạng thái |
Khí không màu, không mùi, không vị |
|
Khối lượng riêng |
Lớn hơn không khí (1,43 g/L ở điều kiện tiêu chuẩn) |
|
Nhiệt độ sôi |
-183 °C |
|
Nhiệt độ nóng chảy |
-218,8 °C |
|
Độ tan trong nước |
Tan ít, tăng khi nhiệt độ giảm |
|
Tính từ |
Oxygen là chất nghịch từ (không bị hút bởi nam châm) |
Tính chất hóa học của Oxygen
Phản ứng với kim loại
- Tạo thành các oxit kim loại như Fe₂O₃, MgO, CuO.
- Phản ứng thường tỏa nhiều nhiệt và làm kim loại cháy sáng hơn.
Phản ứng với phi kim
- Kết hợp với phi kim như C, S, P, H để tạo các oxit phi kim (CO₂, SO₂, P₂O₅, H₂O…).
- Một số phản ứng cần nhiệt độ cao để bắt đầu.
Phản ứng cháy, duy trì sự cháy
- O₂ không tự cháy nhưng thúc đẩy quá trình cháy mạnh hơn.
- Vật liệu trong môi trường giàu Oxygen cháy nhanh, sáng và nóng hơn bình thường.
Tạo Ozone trong điều kiện đặc biệt
- Khi phóng điện mạnh 3O₂ → 2O₃.
- Ozone (O₃) có tính oxi hóa mạnh hơn O₂, thường dùng trong khử trùng và xử lý nước.
Phản ứng oxi hóa hợp chất hữu cơ
- O₂ tham gia quá trình đốt cháy hoàn toàn tạo CO₂ và H₂O.
- Đốt cháy không hoàn toàn có thể tạo CO và muội than.
Điều chế và sản xuất khí Oxygen trong công nghiệp
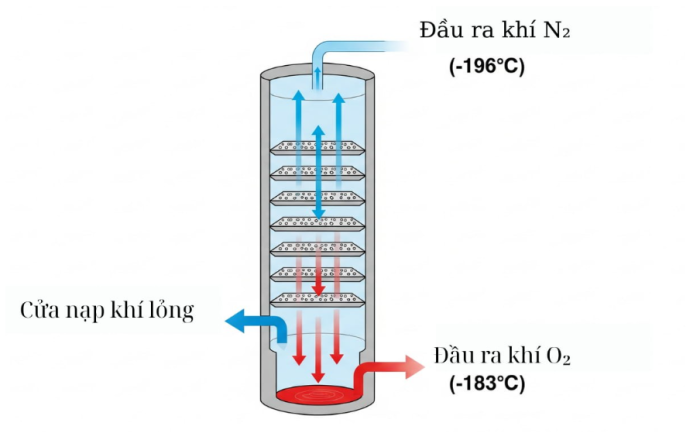
Oxygen công nghiệp được tạo ra chủ yếu bằng phương pháp chưng cất phân đoạn không khí lỏng để đáp ứng nhu cầu tiêu thụ lớn.
- Làm sạch không khí đầu vào nhằm loại bỏ bụi, hơi nước và CO₂.
- Nén và làm lạnh sâu để chuyển không khí từ trạng thái khí sang trạng thái lỏng.
- Đưa không khí lỏng vào tháp chưng cất để tách các thành phần theo nhiệt độ sôi khác nhau.
- Nitrogen bay hơi trước do có nhiệt độ sôi thấp hơn (-196 °C), còn Oxygen với nhiệt độ sôi -183 °C sẽ được giữ lại và thu được dưới dạng Oxygen lỏng tinh khiết.
Khí Oxy có vai trò gì với đời sống?

Hô hấp và sinh tồn
Oxygen là thành phần thiết yếu cho hoạt động sống của con người, động vật và nhiều sinh vật khác. O₂ tham gia vào quá trình hô hấp tế bào, tạo ra năng lượng để duy trì các chức năng của cơ thể.
Y tế và chăm sóc sức khỏe
- Dùng trong thở oxy cho bệnh nhân suy hô hấp.
- Hỗ trợ cấp cứu, phẫu thuật, hồi sức.
- Ứng dụng trong liệu pháp oxy cao áp.
Công nghiệp luyện kim và sản xuất vật liệu
- Tăng hiệu suất và nhiệt độ đốt cháy trong lò luyện thép.
- Dùng trong cắt kim loại bằng oxy,gas.
Công nghiệp hóa chất
- Sản xuất các hóa chất quan trọng như ethylene oxide, methanol, axit sulfuric.
- Tăng hiệu quả phản ứng oxi hóa trong quá trình sản xuất.
Hàng không, vũ trụ, lặn sâu
- Là khí thở trong máy bay, tàu vũ trụ.
- Dùng trong bình khí cho thợ lặn và kỹ thuật dưới nước.
Lưu ý an toàn khi sử dụng Oxygen

Nguy cơ cháy nổ
- Khi tiếp xúc với vật liệu dễ cháy (đặc biệt là dầu mỡ), Oxygen có thể làm ngọn lửa bùng phát mạnh bất thường.
- Dầu mỡ bám trên van hoặc thiết bị Oxygen có thể tự bốc cháy trong môi trường giàu O₂ và áp suất cao, không cần nguồn nhiệt.
- Bình khí nén chứa Oxygen có áp suất lớn, dễ gây nổ nếu va đập mạnh, đặt gần nguồn nhiệt, hoặc sử dụng sai kỹ thuật.
Quy tắc an toàn
- Lưu trữ bình Oxygen ở nơi khô ráo, thoáng mát, tránh xa nguồn nhiệt.
- Dùng thiết bị, van, ống dẫn chuyên dụng cho khí O₂.
- Mở van từ từ để tránh thay đổi áp suất đột ngột.
- Tuyệt đối không để dầu mỡ dính vào van, đầu nối hay tay người thao tác.
- Khu vực làm việc cần thông thoáng và có hệ thống thông gió tốt.
Oxygen (O₂) là một trong những khí quan trọng nhất đối với sự sống và các ngành công nghiệp hiện đại. Từ hô hấp, y tế, luyện kim cho đến hàng không, O₂ đều giữ vai trò thiết yếu. Tuy nhiên, việc sử dụng Oxygen đòi hỏi hiểu đúng về tính chất duy trì cháy mạnh của nó để đảm bảo an toàn tuyệt đối. Nắm rõ các quy tắc vận hành, lưu trữ và sử dụng sẽ giúp khai thác hiệu quả khí O₂ trong cả đời sống và sản xuất.
